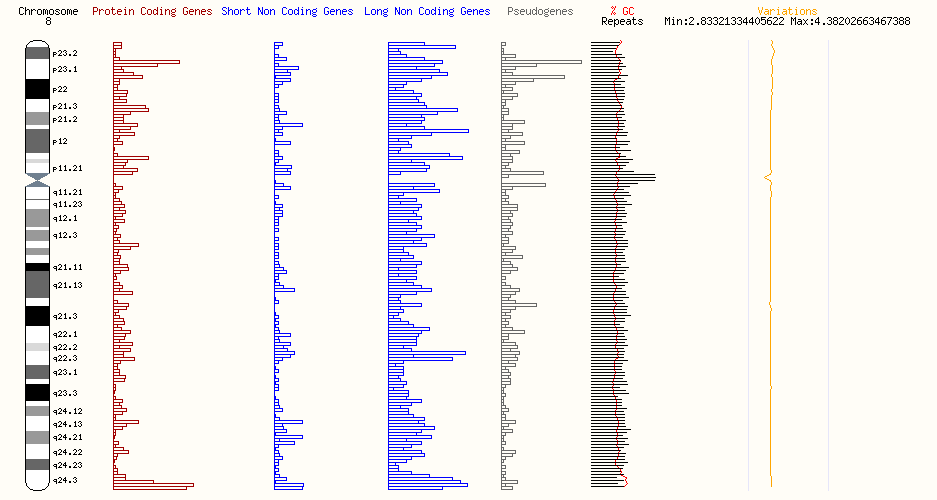
8p23.1領域に位置するBLK、GATA4、FDFT1遺伝子が引き起こす稀少疾患であるMODY(家族性若年糖尿病)、CDH(先天性横隔膜ヘルニア)、SQSD(スクアレン合成酵素欠損症)を臨床特徴、診断、治療の観点から分かりやすく解説します。
この記事のまとめ
本記事では、8p23.1領域に関連する稀少疾患である家族性若年糖尿病(MODY)、先天性横隔膜ヘルニア(CDH)、スクアレン合成酵素欠損症(SQSD)について解説します。これらの疾患に関与する遺伝子BLK、GATA4、FDFT1の役割や症状、診断法、管理の重要性をわかりやすく説明します。
この遺伝子座にある疾患に関与する可能性が高い遺伝子

| S/N | 遺伝子名 | 関連する疾患名 | Associated disease name |
| 1 | BLK | 家族性若年糖尿病 | Maturity-Onset Diabetes of the Young |
| 2 | GATA4 | 先天性横隔膜へルニア | Congenital Diaphragmatic Hernia |
| 3 | FDFT1 | スクアレン合成酵素欠損症 | Squalene Synthase Deficiency |
[1_BLK] 家族性若年糖尿病(Maturity-Onset Diabetes of the Young)


Maturity-onset diabetes of the young (MODY)は、遺伝的要因による非自己免疫性の糖尿病の一群であり、通常、思春期や若年成人期に発症します。BLK遺伝子(染色体領域8p23.1に位置)に起因するMODYは、特にMODY11と呼ばれ、全MODY症例の1%未満を占める極めて稀なタイプです。このタイプのMODYでは、インスリン分泌の異常が病態生理の主要因となっています。
MODYは主に35歳未満で発症し、1型糖尿病や2型糖尿病と異なる特徴を持ちます。1型糖尿病では膵島細胞に対する自己抗体が見られる一方で、MODYではこれらの抗体が見られないことが特徴です。また、発症から数年後(一般的に「ハネムーン期」を過ぎた後)にも内因性のインスリン分泌が持続している場合があります。さらに、MODYでは低用量のインスリン治療(0.5 U/kg/日未満)で血糖値を管理できるケースが多く、インスリンの中断時にもケトアシドーシスが発生しにくいという点も重要な特徴です。

MODYと2型糖尿病を区別するためには、肥満やアカントーシス・ニグリカンス(黒色表皮腫)などが見られないこと、また中性脂肪値が正常であるか、HDLコレステロール(善玉コレステロール)が正常もしくは上昇していることが参考になります。さらに、MODYの患者では安定した空腹時高血糖が見られるものの、薬理学的治療にはあまり反応しない場合が多いです。また、スルホニル尿素薬への極度の感受性を示すこともあります。
遺伝的要因の診断は、家族歴や臨床的特徴から疑われる場合に、分子遺伝学的検査を用いて行われます。家族歴では、糖尿病の発症年齢(通常35歳未満)や、肥満の有無が重要な情報となります。MODYは常染色体優性遺伝を示し、家系内での発症パターンが他の糖尿病とは異なることがあります。たとえば、1型糖尿病は家族内で散発的に見られることが多いのに対し、2型糖尿病は遺伝的要因と環境要因の共有により複数の家族メンバーに発症する傾向があります。

現在、MODYを引き起こす遺伝子として少なくとも14種類が報告されており、その中でもGCK遺伝子(MODY2)やHNF1A遺伝子(MODY3)が最も一般的で、それぞれ全MODY症例の30〜60%を占めます。BLK遺伝子の変異に起因するMODY11は極めて稀ですが、肥満が臨床的特徴として現れることもあります。このような稀なタイプのMODYの診断には、症状や家族歴、実験室検査に基づいた多面的なアプローチが必要です。
MODYの診断と遺伝的原因の特定は、患者自身の治療方針を最適化するだけでなく、家族メンバーへの遺伝カウンセリングや将来発症リスクのある家族の医療的監視にも役立ちます。たとえば、BLK遺伝子関連のMODY11では、臨床的に確定診断を行うために、医学的な詳細な病歴、3世代にわたる家族歴、身体検査、そして分子遺伝学的検査が必要です。
最後に、BLK遺伝子関連MODYは病態生理学的にインスリン分泌の欠陥によって引き起こされます。このため、糖尿病の正確な遺伝的背景を把握することは、適切な治療法の選択において不可欠であり、特に稀少なMODYタイプの患者にとって重要な意味を持ちます。
[2_GATA4] 先天性横隔膜へルニア(Congenital Diaphragmatic Hernia)


先天性横隔膜ヘルニア(CDH)は、単独で発生する場合もあれば、他の先天異常と組み合わせて発生する場合もあります。CDHの原因は多岐にわたり、染色体異常やコピー数変異(CNV)が多くのケースで重要な役割を果たしていますが、これまでにヒトのCDHに明確に関連付けられた単一遺伝子は少数です。本稿では、GATA4遺伝子(8p23.1領域に位置)の変異がCDHの病態形成に関与する可能性について解説します。
CDHは、出生時に重度の呼吸困難として現れることが一般的です。これは、胸腔内への臓器の移動により、肺の発育が妨げられることが主因です。症状の程度は個々に異なり、一部の症例では新生児期を超えて軽度の呼吸器症状や消化器症状が現れる場合もあります。さらに、無症状のまま画像診断で偶然発見されることもあります。

CDHには複数の形態がありますが、代表的なものとして後外側型(Bochdalekヘルニア)が挙げられます。このタイプは、横隔膜の後外側部分が欠損または非常に薄いことで特徴づけられ、多くの場合、胃や腸、肝臓、脾臓などの臓器が胸腔内に入り込んでいます。後外側型はCDH全体の80~90%を占め、その85%が左側、10%が右側、5%が両側性とされています。また、前方型(Morgagniヘルニア)や中央部欠損型といった他の稀なタイプも存在します。
横隔膜の形成異常の背景には、遺伝的要因が深く関わっています。近年の研究では、GATA4遺伝子の変異がCDHに関連していることが示唆されています。GATA4は、細胞の遺伝子発現や分化を制御する亜鉛フィンガー型転写因子で、横隔膜や肺の発生に重要な役割を果たします。この遺伝子の変異は、家族性および孤発性のCDHの両方で確認されており、不完全な発現率(penetrance)が特徴です。例えば、特定の家族で発見されたGATA4の変異(c.754C>T、p.R252W)では、一見正常に見える保因者もMRI検査で軽度の横隔膜欠損が認められました。また、別の孤発性CDH患者からは新生変異(de novo)であるGATA4の変異(c.848G>A; p.R283H)が発見されています。

GATA4遺伝子の影響は、動物モデルを用いた研究でも明らかにされています。例えば、GATA4の発現が妨げられると、横隔膜や肺の欠陥が引き起こされることが確認されています。一方で、レチノイン酸(ビタミンA誘導体)を用いた治療がGATA4の発現を増加させ、横隔膜や肺の発生異常を改善することが示唆されています。このように、GATA4はレチノイン酸経路とも関連しており、横隔膜の発生過程における中心的な役割を果たしていると考えられます。
遺伝的診断技術の進歩により、CDHの原因となる遺伝的変異を特定する能力が向上しています。特に、全エクソーム解析(WES)は、家族性および孤発性CDHにおいて稀な遺伝子変異を特定するための有力な手法です。遺伝的背景を解明することは、患者の診断、治療、予後の評価に大きく寄与します。
CDHの治療は主に外科的修復が中心ですが、呼吸器管理や栄養サポートなどの包括的なケアが必要です。長期的なフォローアップでは、発達の遅れや聴覚障害、胸郭の変形などの合併症がみられることがあり、これらに対応するための専門的な支援が求められます。
CDHは単なる解剖学的欠損ではなく、複雑な遺伝的および発生学的要因が絡む疾患です。特にGATA4遺伝子の研究は、病態の理解と新しい治療法の開発に向けた重要な手がかりを提供しています。今後の研究の進展が、より効果的な診断法や治療法の確立につながることが期待されます。
[3_FDFT1] スクアレン合成酵素欠損症(Squalene Synthase Deficiency)


スクアレン合成酵素欠損症(Squalene Synthase Deficiency, SQSD)は、コレステロール合成過程における稀な先天性代謝異常です。この疾患は、FDFT1遺伝子(8p23.1に位置)に生じた二対性(biallelic)の病的変異によって引き起こされます。以下に、疾患の概要を包括的かつ分かりやすく説明します。
スクアレン合成酵素(SS)は、コレステロール生合成の初期段階を担う酵素で、2分子のファルネシル二リン酸(FPP)をスクアレンに変換する重要な役割を果たします。この酵素の機能不全は、コレステロール合成に不可欠なプロセスを阻害し、多系統にわたる症状を引き起こします。

臨床的には、スクアレン合成酵素欠損症の特徴は、スミス・レムリ・オピッツ症候群(Smith-Lemli-Opitz syndrome, SLOS)に類似した多彩な症状です。具体的には、顔貌異常(狭い額、扁平な鼻根、後方回転耳など)、新生児期に発症する全身性けいれん、脳構造異常(例:脳回形成異常)、視覚障害(視神経低形成、皮質盲)、重度の発達遅滞や知的障害、乾燥肌および光線過敏症、男性における性器異常(停留精巣、尿道下裂)などが挙げられます。また、新生児では低出生体重や黄疸、肝機能異常が見られることがあります。
この疾患は尿代謝プロファイルによって診断が可能です。特に、飽和・不飽和の分枝鎖二カルボン酸やファルネソール由来のグルクロン酸抱合体が増加する独特の尿中代謝物が特徴です。ガスクロマトグラフィー質量分析(GC-MS)や核磁気共鳴分光法(NMRS)でこの特異的なプロファイルを確認することが診断の指標となります。また、分子遺伝学的検査によりFDFT1遺伝子の病的変異を同定することも確定診断の方法です。
治療法については、現在、根本的な疾患修正療法は存在しません。対症療法が主な治療手段となり、けいれん、発達遅滞、便秘、痙縮など各症状に対する標準的な医療が行われます。視覚障害には早期介入、摂食困難には胃瘻の設置が推奨される場合があります。また、睡眠障害が認められる場合には、メラトニンの試用が考慮されます。

予防の観点からは、紫外線や日光暴露を避けることが重要です。乾燥肌や光線過敏症のため、10分程度の日光暴露でも日焼けが生じることがあります。
この疾患は常染色体劣性遺伝形式をとります。患者の兄弟姉妹が同疾患を発症する確率は25%、無症候性保因者である確率は50%です。家族内でFDFT1病的変異が特定されている場合、保因者検査や出生前診断が可能です。
臨床研究では、FDFT1遺伝子の変異がスクアレン合成酵素活性を低下させることが確認されています。これにより、ファルネシル二リン酸が過剰に蓄積し、その代謝物が複雑な代謝経路を引き起こし、細胞成長の抑制やアポトーシスの誘導を含む多様な生物活性を示します。この疾患の研究は、胚形成や器官形成におけるコレステロールの重要性を改めて強調しています。
現在までに報告されている患者は限られており、その多くがヨーロッパ系の家系から特定されています。スクアレン合成酵素欠損症は、臨床的特徴、代謝物プロファイル、遺伝子解析を組み合わせることで診断される稀少疾患ですが、適切な治療とサポートによって患者と家族の生活の質を向上させることが期待されます。
引用文献

- Coman, D., Vissers, L. E. L. M., Riley, L. G., Kwint, M. P., Hauck, R., Koster, J., Geuer, S., Hopkins, S., Hallinan, B., Sweetman, L., Engelke, U. F. H., Burrow, T. A., Cardinal, J., McGill, J., Inwood, A., Gurnsey, C., Waterham, H. R., Christodoulou, J., Wevers, R. A., & Pitt, J. (2018). Squalene synthase deficiency: Clinical, biochemical, and molecular characterization of a defect in cholesterol biosynthesis. The American Journal of Human Genetics, 103(1), 125–130. https://doi.org/10.1016/j.ajhg.2018.05.004
- Coman D, Vissers L, Waterham H, et al. Squalene Synthase Deficiency. 2020 Feb 6. In: Adam MP, Feldman J, Mirzaa GM, et al., editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993-2025. Available from: https://www.ncbi.nlm.nih.gov/books/NBK553533/
- Yu, L., Wynn, J., Cheung, Y. H., Shen, Y., Mychaliska, G. B., Crombleholme, T. M., Azarow, K. S., Lim, F. Y., Chung, D. H., Potoka, D., Warner, B. W., Bucher, B., Stolar, C., Aspelund, G., Arkovitz, M. S., & Chung, W. K. (2013). Variants in GATA4 are a rare cause of familial and sporadic congenital diaphragmatic hernia. Human genetics, 132(3), 285–292. https://doi.org/10.1007/s00439-012-1249-0
- Longoni M, Pober BR, High FA. Congenital Diaphragmatic Hernia Overview. 2006 Feb 1 [Updated 2020 Nov 5]. In: Adam MP, Feldman J, Mirzaa GM, et al., editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993-2025. Available from: https://www.ncbi.nlm.nih.gov/books/NBK1359/
- Naylor R, Knight Johnson A, del Gaudio D. Maturity-Onset Diabetes of the Young Overview. 2018 May 24. In: Adam MP, Feldman J, Mirzaa GM, et al., editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993-2025. Available from: https://www.ncbi.nlm.nih.gov/books/NBK500456/
- Perez, G., Barber, G. P., Benet-Pages, A., Casper, J., Clawson, H., Diekhans, M., Fischer, C., Gonzalez, J. N., Hinrichs, A. S., Lee, C. M., Nassar, L. R., Raney, B. J., Speir, M. L., van Baren, M. J., Vaske, C. J., Haussler, D., Kent, W. J., & Haeussler, M. (2024). The UCSC Genome Browser database: 2025 update. Nucleic Acids Research, gkae974. https://doi.org/10.1093/nar/gkae974
- Harrison, P. W., Amode, M. R., Austine-Orimoloye, O., Azov, A. G., Barba, M., Barnes, I., Becker, A., Bennett, R., Berry, A., Bhai, J., Bhurji, S. K., Boddu, S., Branco Lins, P. R., Brooks, L., Budhanuru Ramaraju, S., Campbell, L. I., Carbajo Martinez, M., Charkhchi, M., Chougule, K., … Yates, A. D. (2024). Ensembl 2024. Nucleic Acids Research, 52(D1), D891–D899. https://doi.org/10.1093/nar/gkad1049

 中文
中文