この記事のまとめ
ミラー・ディーカー症候群(MDS)は、17番染色体の一部欠失によって引き起こされる非常に稀な遺伝性疾患です。滑脳症や特徴的な顔立ち、発達遅延を伴い、患者やその家族に多くの課題をもたらします。本記事では、疾患の概要、診断と管理の方法、そして予後について詳しく解説しています。MDSに関する知識を深め、早期診断と適切なケアの重要性について理解を深めてください。
疾患概要

ミラー・ディーカー症候群(MDS)は非常に稀で重篤な遺伝性疾患で、「隣接遺伝子欠失症候群」として知られています。この疾患は、17番染色体の短腕(17p13.3)に存在する複数の隣接する遺伝子が欠失することで発生します。この欠失には、PAFAH1B1遺伝子やYWHAE遺伝子を含む重要な遺伝子が含まれており、約1.3メガベースの範囲(17番染色体の約1.57 %)にわたる影響が見られます。これらの遺伝子が失われることで、正常な発達が妨げられ、身体的および神経学的にさまざまな問題が引き起こされます。
この疾患の発生率は、出生10万人に1人程度と推定されています。ただし、診断が難しいことや医療従事者の認知度にばらつきがあるため、実際の発生率はこれより高い可能性があります。

MDSの特徴として最も注目されるのが、「滑脳症(タイプI滑脳症)」と呼ばれる脳の発達異常です。滑脳症とは、妊娠中に脳が正常に形成されず、脳表面が滑らかになる状態を指します。この結果、MDSの患者には重度の発達遅延やてんかんがほぼ確実に見られることが報告されています。
さらに、MDSの患者には特徴的な顔立ちがよく見られ、これが臨床診断の大きな手がかりとなります。代表的な顔の特徴としては、突き出た額、こめかみのくぼみ、短く上向いた鼻、下向きに湾曲した上唇の縁、低い位置にあり回転した耳、小さな顎(小顎症)が挙げられます。
病因と診断の方法
ミラー・ディーカー症候群(MDS)は、17番染色体の短腕(17p13.3)に存在する遺伝子の一部が欠失することにより発症する遺伝性疾患です。この「欠失」とは、染色体上の特定の遺伝子が物理的に失われる状態を指し、欠失の範囲は顕微鏡で確認できるほど大きい場合もあれば、非常に小さく、専門的な遺伝子検査を行わなければ検出できない場合もあります。
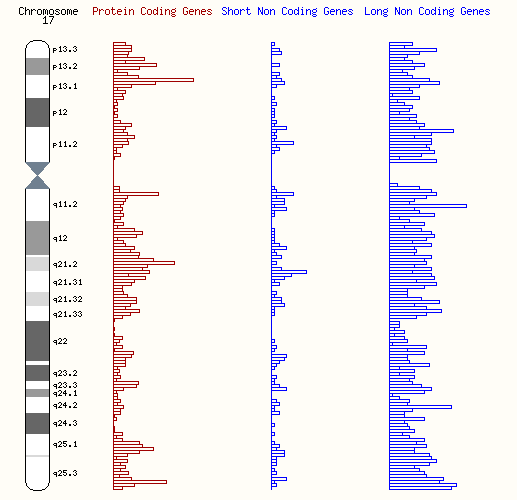
MDSのすべての症例で、必ずLIS1遺伝子(PAFAH1B1)が欠失しています。この遺伝子は脳の発達において極めて重要な役割を果たしており、その欠失によって「滑脳症(lissencephaly)」と呼ばれる状態が引き起こされます。滑脳症では、神経の発達が阻害され、脳表面が滑らかになる結果、重度の発達遅延や神経障害が生じます。
孤発性滑脳症(ILS)では、LIS1遺伝子のみが影響を受けるのに対し、MDSではLIS1遺伝子に加え他の遺伝子も欠失しているため、症状がさらに広範囲に及び、重篤化する傾向があります。研究によると、YWHAE遺伝子の欠失は、MDSの重症度を高める大きな要因であることが示されています。この遺伝子は14-3-3イプシロンというタンパク質をコードしており、その欠失により神経学的および身体的な症状がさらに悪化します。
大脳皮質(思考、記憶、感覚の認識など、重要な機能を担う脳の外層)の発達は非常に複雑なプロセスです。このプロセスは互いに重なり合う3つの主な段階から成り立っています。まず、細胞増殖では、脳細胞が成長し増殖します。次に、神経移動が行われ、これらの細胞が脳内で正しい位置に移動します。そして最後に、皮質組織化の段階で、細胞が互いに接続され、機能的なネットワークとして整理されます。
LIS1遺伝子が異常または欠損している場合、脳細胞が適切な位置に移動する重要な段階である神経移動が妨げられます。このような異常は、滑脳症と呼ばれる状態を引き起こす可能性があります。滑脳症とは、「滑らかな脳」を意味し、発達過程で脳が適切に形成されなかったため、脳表面が異常に滑らかになる疾患です。この状態は、脳が正常に形成および機能しないため、重度の知的障害を含む深刻な発達上の課題を引き起こすことが多いです。
さらに、MDSでは多くの場合、YWHAE遺伝子を含む他の重要な遺伝子も欠失しています。このように複数の隣接する遺伝子が同時に欠失する状態は、「隣接遺伝子欠失症候群」と呼ばれます。この種の疾患では、それぞれの欠失した遺伝子が果たしていた機能が損なわれるため、影響が多岐にわたり、非常に複雑な症状が現れます。
MDSの患者には、特徴的な顔立ち、先天性の異常、発達障害などがしばしば見られます。典型的な症状として、突き出た額、こめかみのくぼみ、短く上向きの鼻、下向きに湾曲した上唇の縁、低い位置で回転した耳、小さな顎(小顎症)などが挙げられます。
最も重症なケースでは、LIS1遺伝子やYWHAE遺伝子に加えてさらに多くの隣接遺伝子が欠失していることがあります。また、一部の患者では、17p13.3の一部が欠失し、他の染色体領域が重複する不均衡な染色体再構成が見られ、症状の複雑さがさらに増します。

症状は、生後0〜23か月の間に現れることが多いです。ミラー・ディーカー症候群の原因となる、顕微鏡で確認できる欠失や非常に小さく顕微鏡では確認できない欠失(微小欠失)は、次世代シークエンシング(NGS)を使用した非侵襲的出生前検査(NIPT)によって高精度かつ安全に検出することが可能です。この検査方法は、母体や胎児に負担をかけることなく実施できる安全性の高い手法として広く認識されています。
超音波検査も、構造的な異常が明確に現れている場合において、ミラー・ディーカー症候群(MDS)の出生前診断に有用な手段です。この方法は胎児の体の構造的な異常を確認する際に役立ち、特に脳や心臓の異常が疑われる場合に重要な情報を提供します。
疾患の症状と管理方法
ミラー・ディーカー症候群(MDS)の管理は、症状の緩和と合併症の予防を中心に行われます。この疾患は多岐にわたる課題を伴うため、複数の専門分野が連携する包括的なアプローチが欠かせません。
食事と栄養管理
MDSの子どもたちは、摂食や嚥下(飲み込む動作)に困難を抱えることが多く、栄養不良や誤嚥性肺炎(食べ物や液体が誤って気道に入り炎症を引き起こす状態)のリスクが高まります。この問題に対処するための方法として、以下が挙げられます:
- 鼻胃管:短期間の栄養補助に使用されます。
- 胃瘻(いろう)チューブ:長期間の栄養補助が必要な場合、特に発育不良や嚥下困難、再発性の誤嚥性肺炎がある場合に推奨されます。
- 定期的に成長の指標を測定し、栄養状態や経口摂取の安全性を評価することが重要です。
けいれんの管理
けいれん発作はMDSの主要な症状であり、継続的な監視と適切な治療が求められます:
- 抗けいれん薬:発作の種類や頻度に基づいて個別に調整されます。
- バルプロ酸とラモトリギンを併用する治療法(ポリセラピー)は、薬剤耐性のあるけいれんの管理に効果的とされています。
- 新たな発作や発達の後退が見られた場合は、速やかに対処するための臨床的な監視が必要です。

便秘と消化器の健康
便秘はMDSで頻繁に見られる問題であり、以下の方法で対処できます:
- 便軟化剤、消化管運動促進薬、浸透圧性下剤、またはその他の下剤を必要に応じて使用します。
- 消化器の不快感や誤嚥による呼吸不全の兆候を定期的に評価することが重要です。
発達支援と感覚機能のサポート
MDSの子どもたちは、発達の遅れや感覚障害を抱えることが多いため、医療的および教育的な支援が必要です:
- 知的障害、筋緊張亢進(体が硬くなる状態)、視覚障害、聴覚障害に対する治療やカウンセリングは、生活の質を向上させる上で重要です。
- 発達の進行状況、移動能力、自立した生活スキルを評価し、それに基づいた介入を行います。
- 学習支援や環境への適応を促進するために、教育評価を行い、適切なプログラムを提供します。
定期的なモニタリングと専門家による評価
定期的な検査や専門的な評価により、進行状況を追跡し、新たな問題の早期発見が可能になります:
- 成長や栄養状態の評価を定期的に実施します。
- 眼科検査や聴覚検査は、毎年または必要に応じて行い、視覚および聴覚の問題に対応します。
- 呼吸器の問題や異常な発作、発達の後退などの兆候がある場合、速やかに医療対応を行います。
将来の見通し
ミラー・ディーカー症候群(MDS)の子どもたちにおける発達の見通しは、残念ながら厳しいものとされています。多くの場合、2歳を迎える前に命を落とすことが多く、10歳まで生存できるお子さんはごく少数です。これまでの記録では、MDSの患者さんで最も長く生存されたのは17歳でした。
一方、PAFAH1B1遺伝子のみが影響を受けた滑脳症では、MDSに比べてやや良い見通しが報告されています。それでも限界は多く、約50%の患者さんが10歳を迎えることができますが、20歳を超えて生存される方は非常に稀です。最長生存記録は、30歳まで生存された例です。
これらの情報から、MDSおよび関連する滑脳症が非常に重篤な疾患であることがわかります。そのため、これらの疾患においては、早期の診断と適切な症状管理、そしてお子さんやご家族の生活の質を少しでも向上させるための支援が重要となります。
もっと知りたい方へ
【写真あり・英語】ユニーク(Unique)による17p13.3欠失症候群に関する情報 パンフレット

 中文
中文